微信在线咨询
微信在线咨询

| 产品编号 | 产品名称 | 产品包装 | 产品价格 |
| C0271S | 内毒素检测试剂盒(鲎试剂动态浊度法) | 34次 | 468.00元 |
碧云天研发生产的内毒素检测试剂盒(鲎试剂动态浊度法),即Kinetic Turbidimetric LAL Endotoxin Assay Kit,是一种基于鲎试剂酶促凝集反应形成凝胶,使反应液浊度(吸光度)增加的原理,定量检测细菌内毒素(endotoxin)也称脂多糖(Lipopolysaccharide, LPS)的超高灵敏度、高稳定性、更宽检测范围的常用试剂盒[1, 2]。检测灵敏度下限可以低达0.01EU/ml,上限可高达10EU/ml,极大扩宽了高浓度范围的检测能力;并且可以检测微量样品,样品的体积可以仅为50微升或更小体积。
本产品和碧云天的内毒素检测试剂盒(鲎试剂一步显色法) (C0273)、内毒素检测试剂盒(鲎试剂显色法) (C0276)和内毒素检测试剂盒(鲎试剂显色法改进版) (C0278)相比仅需经过一步内毒素检测试剂与待测样品的混匀步骤,缩短了操作时间,并且检测灵敏度基本一致,可低至0.01EU/ml,而检测上限可达10EU/ml,具有更宽的检测范围[3];但本产品需要使用酶标仪或其他带有温控孵育系统并可连续动态检测340nm、405nm或630nm处波长吸光度的光学检测仪器。对于样品自身有一定颜色的情况,优先推荐使用内毒素检测试剂盒(鲎试剂显色法) (C0276)或内毒素检测试剂盒(鲎试剂显色法改进版) (C0278)。
本试剂盒首次启用后,适当保存至少在2个月内有效。基于鲎试剂的内毒素检测试剂盒,通常只能配制后立即使用,导致试剂盒的浪费。本试剂盒经过精心优化,确保首次配制成溶液后,按照说明书推荐的方法保存,至少2个月内有效。
本试剂盒操作简单便捷,样品需求量小,灵敏度高,检测范围宽。本试剂盒操作简单快速,检测试剂直接加入到待测样品中并混匀,即可进行37ºC孵育和吸光度连续动态检测,从而实现简单、快速、高灵敏地检测内毒素含量;样品需求量小,每个反应体系仅需50μl或更小体积的待测样品;检测灵敏度高、测定样品的线性范围宽,检测内毒素浓度范围为0.01-10EU/ml [1, 2]。
用途:溶液样品中内毒素污染检测;注射用药物、生物制品和医疗器械产品等各种不同类型样品中内毒素含量的定量检测。
原理:鲎试剂为鲎科动物东方鲎的血液变形细胞裂解物的冷冻干燥品(Lyophilized Amebocyte Lysate, LAL)或体外重组的同类试剂,含有C因子、B因子、凝固酶原、凝固蛋白原等。在适宜的条件下(温度,pH值及无干扰物质),内毒素激活C因子,引起一系列酶促反应,使鲎试剂产生凝集反应形成凝胶,进而导致反应液浊度即吸光度(OD值)的增加。待测样品内毒素浓度与反应液浊度或吸光度增加的速度成正相关,与浊度或吸光度(OD值)上升某一预设限值(启动OD,即起始OD与目标OD的差值)所需的时间(定义为启动时间T)成负相关,启动时间的对数与内毒素浓度的对数成线性关系。鲎试剂动态浊度法就是根据此原理,通过检测反应液浊度上升至某一预先设定的吸光度所需的反应时间,或是检测反应液浊度增加的速度来定量测定样品中的内毒素浓度[1, 2]。
检测灵敏度高,检测范围宽。最低检测限可以达到0.01EU,最高可达到10EU。具体的检测效果请参考图1。
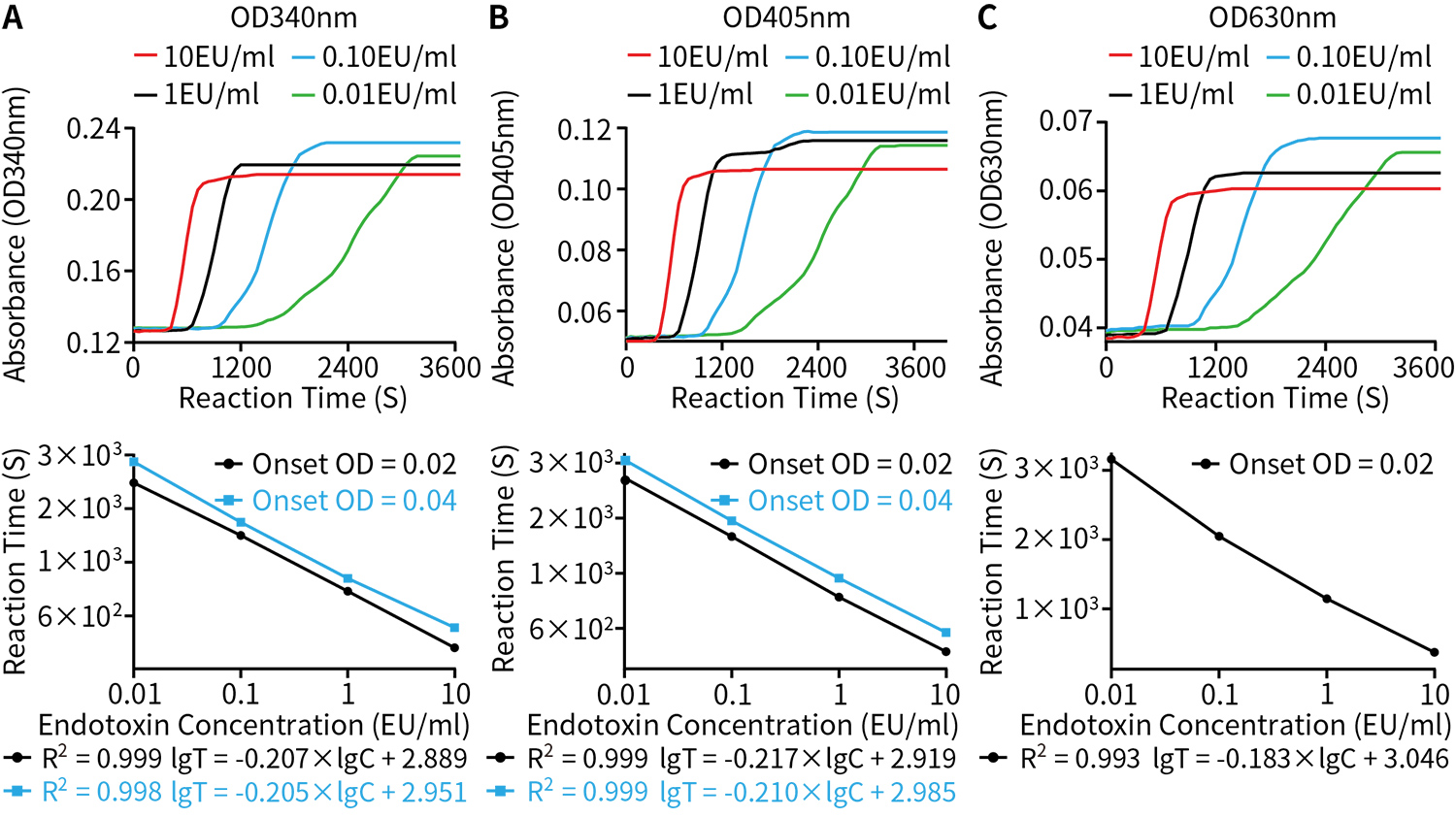
图1.碧云天生产的内毒素检测试剂盒(鲎试剂动态浊度法) (C0271)检测效果图。取配制好的下列浓度的内毒素标准品溶液:0.01、0.10、1.00、10.00EU/ml各50μl,用本试剂盒和BeyoGold™超低吸附96孔板(平底带盖,独立包装) (FULA961)进行检测反应及标准曲线的绘制。图A为在340nm波长条件下进行吸光度连续动态检测的效果及所绘制的标准曲线(启动OD分别设为0.02和0.04);图B为在405nm波长条件下进行吸光度连续动态检测的效果及所绘制的标准曲线(启动OD分别设为0.02和0.04);图C为在630nm波长条件下进行吸光度连续动态检测的效果及所绘制的标准曲线(启动OD设为0.02)。其中,样品内毒素浓度(C)为横坐标,孵育反应时间(T)为纵坐标,标准曲线由lgT和lgC拟合绘制而成。实际检测时会因检测仪器等实验条件的不同而存在差异,图中数据仅供参考。
一个包装的本试剂盒共可以检测34个样品(含标准品)。
包装清单:| 产品编号 | 产品名称 | 包装 |
| C0271S-1 | 内毒素标准品(100EU) | 1管 |
| C0271S-2 | 内毒素检测试剂 | 1瓶 |
| C0271S-3 | 内毒素检测试剂配制液 | 3ml |
| C0271S-4 | 内毒素检测用水 | 50ml |
| — | 说明书 | 1份 |
4ºC保存,两年有效。内毒素检测试剂溶解后须立即适当分装,-20ºC保存一周有效,经液氮速冻后-80ºC保存至少两个月有效。内毒素标准品溶解后-20ºC保存,至少6个月有效。
注意事项:内毒素检测试剂溶解后很不稳定,需要尽量在10分钟内使用完毕或适当分装后保存。因此试剂盒在使用过程中需要预先做好各项准备工作,在需要加入内毒素检测试剂前再溶解内毒素检测试剂,或解冻之前分装冻存的内毒素检测试剂。
本产品所提供的内毒素检测用水请在首次开启后建议立即使用完毕,或务必在无内毒素实验条件下,使用无内毒素实验耗材对其适当分装并保存于-20ºC。常规实验室条件下,反复多次取用同一容器中的内毒素检测用水,极易因环境因素造成内毒素的污染。
请务必使用首次开启的内毒素检测用水或分装后确保无内毒素污染的内毒素检测用水,或自行准备的确保无内毒素的超纯水进行内毒素检测所需试剂的溶解和配制,以免造成试剂的外源内毒素污染。
所有内毒素检测的实验过程均需在无内毒素条件下,使用无内毒素实验耗材进行,否则极易对内毒素检测造成干扰。
实验所用的器皿需经预处理,以去除可能存在的外源性内毒素,常用的方法是在250ºC干烤至少60分钟,也可以采用其它确保不干扰细菌内毒素检查的适宜方法。若使用塑料器械,应选用表明无内毒素并且对实验无干扰的器械。
实验操作过程应防止微生物的污染。
溶解并稀释后的内毒素标准品溶液静置时间若超过10分钟,使用前应在旋涡振荡器上振荡混匀1分钟。冻存的溶解后的内毒素标准品,下次使用时须先充分溶解,并剧烈涡旋混合后使用。
本试剂盒中的内毒素检测试剂溶解后,须立即适当分装,-20ºC保存一周有效,经液氮速冻后-80ºC保存至少两个月有效。务必避免反复冻融。
内毒素检测所需试剂在溶解配制好后,如不能一次性使用完,请立即使用无内毒素的耗材进行分装冻存,随用随取。
同一管检测试剂在常规实验条件下多次反复取用后,也极易造成环境中内毒素的污染,建议根据实验需求对试剂进行适当分装。
推荐设置不添加待测样品的空白对照,以确认整个检测体系是否被环境内毒素所污染。
样品的稀释和制备,推荐使用本试剂盒提供的内毒素检测用水或碧云天的无内毒素超纯水BeyoPure™ Ultrapure Water (Sterile, Endotoxin-Free) (ST878)。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
| 内毒素浓度(EU/ml) | 加入内毒素检测用水体积(ml) | 加入内毒素溶液浓度(EU/ml) | 加入内毒素溶液体积(ml) |
| 10.00 | 0.9 | 100.0 | 0.1 |
| 1.00 | 0.9 | 10.0 | 0.1 |
| 0.10 | 0.9 | 1.0 | 0.1 |
| 0.01 | 0.9 | 0.1 | 0.1 |
| 试剂 | 阴性对照 | 内毒素标准品 | 待测样品 |
| 内毒素检测用水(μl) | 50 | ||
| 内毒素标准品溶液(μl) | 50 | ||
| 待测样品(μl) | 50 | ||
| 内毒素检测试剂溶液(μl) | 50 | 50 | 50 |
| 混匀,37ºC孵育并测定340、405或630nm吸光度,每30-60秒测定一次,连续测定1-2小时。 | |||
| 产品编号 | 产品名称 | 包装 |
| C0221B | PBS (pH7.4, Low Endotoxin, Cell Culture Grade) | 500ml |
| C0268S/M | Protein Endotoxin Removal Kit | 200次/1000次 |
| C0271S | 内毒素检测试剂盒(鲎试剂动态浊度法) | 34次 |
| C0273S | 内毒素检测试剂盒(鲎试剂一步显色法) | 200次 |
| C0276S | 内毒素检测试剂盒(鲎试剂显色法) | 160次 |
| C0278S | 内毒素检测试剂盒(鲎试剂显色法改进版) | 400次 |
| ST876-100ml/500ml | BeyoPure™ Ultrapure Water (DNase/RNase-Free, Sterile) | 100ml/500ml |
| ST878-100ml/500ml | BeyoPure™ Ultrapure Water (Sterile, Endotoxin-Free) | 100ml/500ml |









 微信在线咨询
微信在线咨询